ミセル可溶化を支配するものはなに? −タコが入りやすいタコ壷の話−
【研究ノート】
稲葉 一穂
アルミ缶とスチール缶を見分けたり、食べ残しのご飯粒を古いストッキングで漉し取ったり…。家事をしている(させられている)方々なら、分別の大変さはお解りいただけることと思いますが、これが水に溶けている重金属イオンや化学物質だったら…。とても大変な作業です。筆者は、平成4年からアリゾナ大学と、平成17年から日本原子力研究開発機構と共同で、水に溶けている重金属や化学物質の分離回収法の研究を行っています。このような目的には、有機溶剤を利用した溶媒抽出法が従来から使用されていましたが、有機溶剤は毒性や可燃性の危険があることから、新たな媒体の開発が必要です。様々な新規媒体の利用が研究されていますが、私達は、界面活性剤ミセルに注目して研究を行っています。
界面活性剤とは、一つの分子の中に水に溶けやすい部位と水に溶けにくい(油に溶けやすい)部位を備えた分子のことで、合成洗剤の主成分です。単分子としては水の中で不安定なため、100分子程度が集合して、水に溶けにくい部位を内側に、親水性基を水相に突き出した、ミセルと呼ばれる楕円球形の会合体を生成して安定化します。この会合体の中心部は油と同じような性質のため、水に溶けにくい物質を溶解する(ミセル可溶化)ことが知られています。これが合成洗剤の洗浄力の一つの源となっているのです。
「原子力」「洗浄」とキーワードが並ぶと、何やらホットな話題を想像してしまいますが、勿論その方面も含めて、ラボスケールの分離分析から、地下水中の有機塩素系溶剤の除去まで、様々な環境問題への応用が期待できるのです。
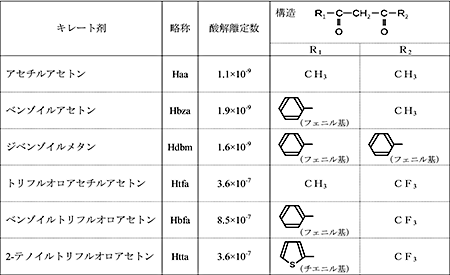
共同研究の中で、筆者は、どのような分子が、どのようなミセルに、どの程度、どのくらいの速度で溶け込んでいくのかを明らかにすることを担当しています。実験と解析を簡便にするために、分子イオンを生成しない非イオン性界面活性剤ミセルを使用し、可溶化量が発色量から測定できる、鉄(III)キレート錯体をモデル溶質として研究しています。使用したキレート剤の構造と酸解離定数を、表1に示します。
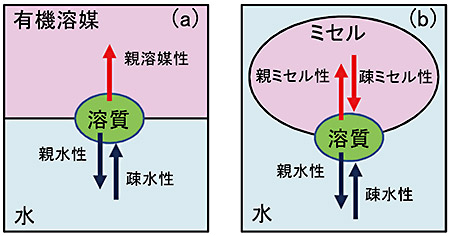
一般に、水と有機溶媒の間の溶質の分配は、図1(a)で示すような3つの因子で説明できます。ここで、親××性は、水和や溶媒和のような溶質-溶媒相互作用による溶けやすさを示し、強い酸や不飽和性の高い錯体で大きくなります。疎××性は、溶媒-溶媒ネットワークからの溶質の除かれやすさを意味し、サイズが大きいものや、水や溶媒に濡れにくいものほど大きくなります。有機溶媒がヘキサンのような無極性溶媒では、親水性と疎水性が、アルコールやエーテルのような溶媒和型溶媒では、これら3つの因子が関与することが知られています。
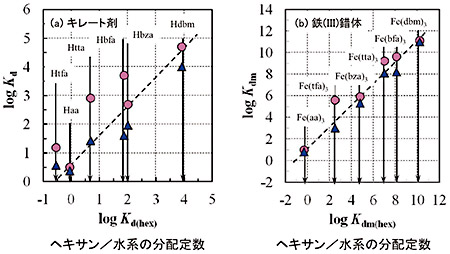
例として、溶媒和型有機溶媒であるジエチルエーテル/水系と、代表的な界面活性剤ポリエチレングリコール-t-オクチルフェニルエーテル(TritonX-100)の作るミセル/水系での、キレート剤(K d)および錯体(K dm)の分配定数(=[溶質](solvent)/[溶質](water))を、ヘキサン/水での分配定数(K d(hex)、K dm(hex))と比較したものを図2(a)と(b)に示します。溶質-溶媒相互作用の小さいHaa、Hbza、Hdbm とその錯体は、ジエチルエーテル/水系とヘキサン/水系で大きな差はありません(破線)が、これら6種の中では強い酸であるHtfa、Hbfa、Htta とその錯体では、溶質-溶媒相互作用の影響で、ジエチルエーテル/水系では大きな値を示しています(●)。一方、Triton X-100 ミセル/水系(▲)では、ジエチルエーテルとは異なるパターンを示しています。そして、嵩高いフェニル基(C6H5-)と、水に濡れにくいトリフルオロメチル基(CF3-)を持つHbfa とその錯体では、特に分配定数が小さくなっていることが分かります。これは、これらの溶質が、ミセルに入り込みにくいことを意味しています。
一方、ミセルへの錯体の侵入と脱離の速度は、不思議な傾向を示します。メチル基(CH3-)をフェニル基に置換すると、嵩高くなるために水に溶けにくくなり、ミセルへの侵入速度は大きくなり、脱離速度は小さくなります。ところが、メチル基をトリフルオロメチル基に置換すると、水に濡れにくくなるために水に溶けにくくなりますが、侵入速度は小さくなります。そして、不思議なことに、ミセルからの脱離速度も小さくなるのです。そして、フェニル基を同じくらいの嵩高さを持つチエニル基(C4H3S-)に置換すると、侵入速度も脱離速度も増加するのです。
これらの現象は、ミセル内部の構造が関与していると考えられます。ミセルは構成する界面活性剤分子の構造から、中心部と外殻部で性質の異なる二重構造となっており、中心部はヘキサン類似ですが、ミセル外殻部には、界面活性剤分子の3~5倍当量の水分子が溶解し、オキシエチレン鎖との間で高度な水素結合のネットワークを構成していると考えられています。この水素結合ネットワークが障壁となって、水に濡れにくいトリフルオロメチル基を持つ溶質の侵入(通過)を制限していると考えられます。チエニル基は、水素結合可能なイオウ原子を持っているため、外殻部の水素結合ネットワークが障壁にはならないのだと考えられます。このように、ミセルを利用した抽出系では、これまでの有機溶媒抽出系とは異なる因子(疎ミセル性)にも支配されていることが分かってきました(図1(b))。
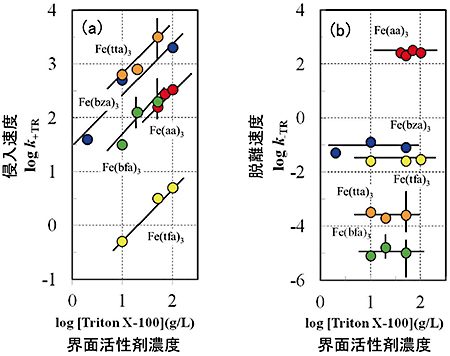
さて、いろいろ研究内容を説明してきましたが、そもそもミセルって本当にいつも同じ形と大きさで存在しているのでしょうか?これまで、粘度測定やスペクトル分析などから、ミセルを構成する分子数の報告などがなされていますが、信用できるのでしょうか?その答えが図3です。これは、今回検討した鉄(III)錯体が、水からミセルへと入り込む速度(k +TR)と、ミセルから水へと脱離する速度(k -TR)を、界面活性剤添加濃度の依存性で示したものです。ミセルへの侵入速度(図3(a))は界面活性剤濃度に比例しますが、脱離速度(図3(b))は界面活性剤濃度に依らず一定となっていることが分かります。侵入反応では、水の中の移動が律速でないなら、侵入速度は水とミセルの界面積に比例しますが、界面活性剤濃度と界面積が比例するのは、粒子サイズが濃度に依らず一定の場合のみです。一方、ミセルから脱離する場合、界面活性剤濃度が変化しても、脱離速度が一定となるのは、ミセルのサイズが濃度に依らず一定で、脱離する分子一つ一つについては脱離条件の変化がない場合に限られます。つまり、これらの結果は、ミセルのサイズが一定であることを示しているのです。
このような、「溶質の出入り」を利用して、ミセルのサイズと構造が変化しないことを証明したのは、この研究が世界で最初です。しかし、「地球規模の研究」と比較すると、いかにもタコ壷の隅をつつくようなちっぽけな世界の研究で、何の役に立つの?という批判が聞こえてきます。それでも、タコ壷の大きさや入り心地を調べておかなければ、タコは捕れません。いつの日か、このような基礎研究をベースとした汚染浄化の技術が開花し、効率よくタコ(汚染物質)が捕れるようになることを夢見て、今日も私は「タコ壷研究」に励んでいるのです。
水環境管理研究室長)
執筆者プロフィール:

昭和60年4月に、27歳で国立公害研(当時)に入所しました。いよいよ来年度からは、人生の半分以上が環境研職員となります。 学生時代は、四塩化炭素中での配位子交換反応の速度論研究など、「理想的な溶液」ばかりを扱ってきましたが、入所してからは、手賀沼、綾瀬川から団地の排水まで、様々な「現実的な水」を扱うようになりました。現場の水から学んだことはいろいろありますが、採水調査の際に素手で水を汲めるかどうか、その手を洗わずに昼食のおにぎりが食べられるかどうかが、「名水」と「迷水」を分ける分水嶺だと判ったのも、27年間の収穫の一つです。